脂质体载药咨询问价
酸性环境(pH值2.0-4.0)通常⽤于产⽣⽤于活***物装载的跨膜pH梯度。在37℃和pH2.0条件下,SM/Chol脂质体(55/45,mol/mol)的⽔解速率⽐DSPC/Chol脂质体慢约100倍。此外,含有SM/Chol的脂质体表现出比较好的药代动⼒学特性,即增加循环时间并增强药物向靶组织的递送。胆固醇(Chol)是脂质体双分⼦层的另⼀个主要成分,⼏乎可以⽤于所有的商业产品。Chol的加⼊可以促进脂链的堆积和双分⼦层的形成,调节膜的流动性/刚性,并进⼀步影响药物释放、脂质体的稳定性和胞外分泌动⼒学。对于Shingrix(带状疱疹疫苗,含有糖蛋⽩E抗原和AS01B脂质体佐剂系统)的产物,Chol可以避免QS21(AS01B佐剂系统中的免疫增强剂之⼀)以2:1的⽐例(Chol:QS21,w/w)⽔解。对于AmBisome的产物,与⾮甾醇相⽐,Chol降低了脂质体制剂的毒性。Chol对双分⼦层性质的影响是浓度依赖性的。据报道,低浓度(2.5mol%)和⾼浓度(>30mol%)的Chol对脂质双分⼦层的性质影响不⼤。5<Cholmol%<30的Chol的“冷凝效应”或“有序效应”导致颗粒⼤⼩从220nm逐渐增⼤到472nm,膜的流动性降低,药物释放减少。除了Chol,其他与Chol结构相似的甾醇,如⻩体酮、⻨⻆甾醇和⽺⽑甾醇,也被研究⽤于调节膜的刚性和稳定性。脂质体表⾯修饰的作用。脂质体载药咨询问价
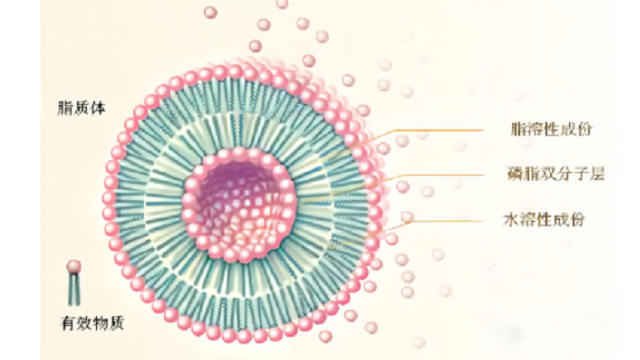
脂质体靶向递送中RGD配体修饰尽管阳离子脂质体具有在体内递送核酸的潜力,但其递送到特定靶点仍然是一个主要挑战。为了增强携带核酸的阳离子脂质体在靶组织中的分布,研究人员用多肽和小分子修饰了脂质体表面。例如,研究了Arg-Gly-Asp(RGD)肽修饰的脂质体增强核酸向整合素受体表达细胞传递的能力。负载P糖蛋白特异性siRNA的RGD修饰阳离子脂质体对整合素受体表达的人乳腺*MCF7/A细胞的递送率更高,导致P糖蛋白的***沉默。与此一致的是,分子成像显示,与小鼠模型的邻近正常组织相比,MCF7/A**组织中RGD修饰的阳离子脂质体和siRNA的分布更高。在**近的一项研究中,用环RGD和辛精氨酸修饰脂质体表面,以利用环RGD的整合素受体结合效应和辛精氨酸的细胞穿透效应。双配体修饰的阳离子脂质体增加了整合素avb3表达细胞的细胞摄取,并且更有效地转染荧光素酶编码质粒DNA。脂质体载药咨询问价聚乙二醇在免疫脂质体中起到了重要作用。
质粒DNA脂质体质粒DNA要在细胞内被有效地翻译,质粒DNA必须经过有效的细胞内运输进入细胞质,并从细胞质进入细胞核。编码白细胞介素12(一种具有抗**活性的细胞因子)的质粒DNA与阳离子脂质体配合,并在转移性肺*小鼠模型中测试其体内***作用。所研究的阳离子脂质体由全反式维甲酸(增强抗肿瘤作用)、DOTAP和胆固醇(摩尔比10:0.5:0.5)组成,与编码白介素12的质粒DNA配合。2次静脉注射质粒DNA(1.2mg/kg/只)后,与对照组相比,**结节和肿瘤细胞数量减少。在另一项研究中,应用由O,O-ditetradecanoyl-N-(α-trimethyl-ammonioacetyl)diethanolaminechloride(DC-6-14)、DOPE和胆固醇组成的阳离子脂质体递送表达miRNA7的质粒DNA。在携带酪氨酸激酶抑制剂耐药的异种移植**的小鼠身上测试了脂质体的***效果。**内注射阳离子脂质体复合物包封质粒(每只小鼠3ug)与注射乱码miRNA质粒DNA脂质体的小鼠相比,***抑制**生长。
脂质体各组分对核酸递送效率的影响对于使用阳离子脂质体开发核酸***剂,一个先决条件是必须将核酸适当地递送到靶细胞并到达适当的亚细胞区室(例如,细胞质或细胞核)。已知阳离子脂质体的递送效率会受到阳离子脂质和辅助脂质类型及其组成的影响。阳离子脂质是纳米粒子的**成分,具有一个带正电的头基和一个或两个由碳氢链或类固醇结构组成的疏水尾区的共同结构。Felgner和同事报道了N-[1-(2,3-二聚氧基)丙基]-N,N,N-三甲基氯化铵(DOTAP)的合成,其具有一个单价阳离子头和两个碳氢化合物尾部,并用于制备小的单层脂质体。他们将DNA包裹的脂质体转染到小鼠L细胞中,并证明阳离子脂质中和了带负电荷的DNA,使阳离子脂质体有更好的机会与带负电荷的细胞膜相互作用。从那时起,各种阳离子脂质和基于脂质的纳米颗粒被设计和评估用于核酸的细胞递送,包括DNA,siRNA,miRNA和AS-ODN。这些新的阳离子脂质已经通过文库技术和基于理性的预测相结合的方法被鉴定出来。对类脂类材料文库的筛选产生了由十个碳和两个烷基链组成的阳离子脂质,发现其比其他候选物更有效。
由于在巨噬细胞上发现了甘露糖受体, 因此甘露糖已被用于修饰阳离子脂质体以靶向巨噬细胞递送。

基因递送用脂质体随着科学技术的进步,与人类基因组及其在疾病***中的应用相关的各种发现变得更加触手可及。尽管有了这些发展,选择一个合适的载体将基因传递到目标是至关重要的。其中一种重要的载体是脂质体,它可以将DNA、反义寡核苷酸、siRNA和其他潜在的药物输送到细胞核中。专门设计的脂质体如阳离子脂质体、pH敏感脂质体、融合性脂质体和基因体被用于基因递送研究。由于DNA带有强烈的负电荷,因此转染细胞变得非常困难。DNA进入细胞核可以用不同的方法进行。它们大致可分为物理、化学、生物和机械。使用脂质体传递DNA属于化学范畴。阳离子脂质体作为DNA转染载体已显示出良好的效果。然而,可以观察到,转染效果比较好的脂质有三个主要成分:带正电荷的头基团与带负电荷的DNA相互作用,决定脂质溶解度的连接基团和有助于将脂质锚定在双分子层上的疏水性基团。脂质DNA络合是由于脂质表面的阳离子电荷使DNA静电吸附而形成的。内容物的递送可能归因于阳离子脂质体的膜融合,同时避免了核仁和溶酶体对DNA的降解。脂质体的大小是res***的重要决定因素。在这方面,当脂质体用于基因递送时,内皮细胞的通过是***道屏障。基因转移**重要的靶***是肝脏。核酸与化学增敏剂在阳离子脂质体共同递送。脂质体载药咨询问价
固体脂质纳米颗粒和纳米结构脂质载体的区别。脂质体载药咨询问价
脂质体核酸疫苗的稳定性和储存性脂质纳米颗粒-mrna制剂的储存条件是其临床转化的重要考虑因素,因为储存(水、冷冻和冻干储存)和冷冻保护剂(蔗糖、海藻糖或甘露醇)的类型会影响脂质纳米颗粒-mrna制剂的长期稳定性168。例如,将5%(w/v)的蔗糖或海藻糖添加到脂质纳米颗粒-mRNA配方中,储存在液氮中,可以维持mRNA在体内至少3个月的递送效率168。值得注意的是,授权的COVID-19mRNA疫苗都是在蔗糖存在的冷冻条件下储存17。mRNA-1273保存在-15°C至-20°C,解冻后直接注射17,而BNT162b2保存在-60°C至-80°C,注射前需要解冻和生理盐水稀释17。**近,根据新的稳定性数据,欧洲药品管理局(EMA)已批准BNT162b2在-15°C至-25°C下储存2周。尽管冷链运输可以维持疫苗活性,但不需要冷藏或冷冻储存的脂质纳米颗粒-mrna制剂的开发不仅可以降低生产和运输成本,还可以加快疫苗接种过程。因此,研究影响脂质纳米颗粒-mrna配方长期储存的因素是很重要的。脂质体载药咨询问价
上一篇: 微泡荧光染料细胞膜
下一篇: 四川红色荧光脂质体载药