陕西脂质体载药mRNA
2脂质体的主要成分
⽢油磷脂(GP)、鞘磷脂(SM)和胆固醇(Chol)是市场上脂质体产品中使⽤的基本成分。GP含有⽢油,它连接⼀对疏⽔脂肪酸链和⼀个亲⽔极性头基。脂肪酸和极性头基团的类型。在⽣理pH下,不同的头部组提供负(PA、PS、PG和⼼磷脂)或中性(PC和PE)电荷的脂质体。带负电的DSPG⽤于AmBisome(注射⽤两性体脂质体),可与带正电的AmpB胺基相互作⽤,形成稳定的离⼦配合物,⽽⽤于Vyxeos的DSPG通过强⼤的库仑斥⼒使脂质体聚集**⼩。⽤于DaunoXome(柠檬酸柔红霉素脂质体注射液)、Onivyde(伊⽴替康脂质体注射液)和Vyxeos的DSPC是⼀种中性合成脂质,具有明确的脂肪酸组成(两分⼦硬脂酸)、⾼纯度和相对⾼的相转变(Tm为55◦C)。EPC作为赋形剂加⼊Myocet和Visudyne(维替泊芬粉为输液溶液)中。EPC是从蛋⻩中纯化的天然磷脂(NPL)。与半合成脂和合成脂相⽐,NPL的⽣产成本较低,但转变温度较宽,难以获得完全相同的NPL,并且脂质体可能存在批次差异。此外,EPC的不饱和脂肪酸导致了−15~−5◦C的低相变温度,表明脂质体双分⼦层在体温中处于⽆序和药物“漏出”状态。 脂质体的载药率怎么计算。陕西脂质体载药mRNA
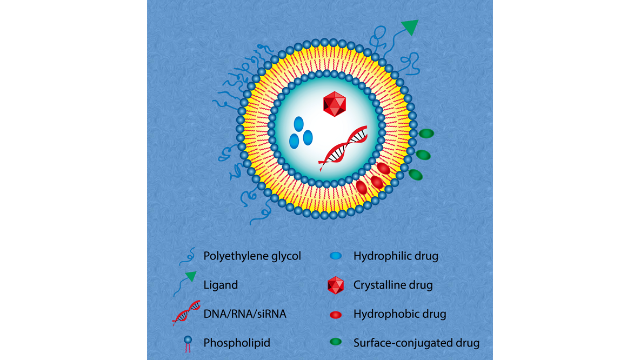
脂质体的稳定性和储存是确保其在制备后能够长期保持其结构完整性和功能性的重要方面。以下是确保脂质体稳定性和适当储存的一些关键考虑因素:1.温度控制:脂质体通常对温度敏感,因此在储存和运输过程中需要严格控制温度。通常,脂质体应存储在冰箱或冷冻条件下,避免高温和冻结2.光照保护:脂质体对光敏感,容易被紫外光照射破坏,因此应该避免直接阳光照射。可以选择不透光的容器进行储存,或者使用防紫外线包装材料。3.惰性气体保护:氧气和水分对脂质体稳定性有不利影响,因此在储存过程中,可以采用惰性气体(如氮气)保护,减少氧气和水分的接触4.pH值控制:某些脂质体制剂对pH值敏感,因此在储存过程中需要控制环境的酸碱度。通常,脂质体应存储在中性或略微酸性的条件下5.防止冻融循环:避免反复冻融会影响脂质体的结构和稳定性,因此在储存和运输过程中应尽量避免冻融循环6.定期检查和测试:定期对储存的脂质体样品进行检查和测试,包括外观检查、粒径分布、稳定性测试等,以确保其质量和性能符合要求。合理的储存条件和定期的质量检查是确保脂质体稳定性和储存的关键。通过适当的控制和管理,可以延长脂质体的保质期,并确保其在使用时能够发挥良好的药物传递效果。陕西脂质体载药mRNA被动载药⽅法是在脂质体制备过程中对药物进⾏包封的方法。

脂质体的Zeta电位Zeta电位被认为是影响细胞摄取和药物传递的重要因素之一。与带电系统相比,膜紧密包裹的中性电荷脂质体往往在循环中停留更长时间,并表现出更高的药物保留率。某些血浆蛋白对脂质体具有亲和力如果脂质体带电,这种亲和力就会增强。特别是阳离子系统有望迅速与体循环中的各种成分相互作用,从而在体内具有更短的半衰期。众所周知,阴离子脂体含有带负电荷的脂质,如磷脂酰丝氨酸(PS)、磷脂酰二酸(PA)和磷脂酰甘油(PG),会被巨噬细胞吸收,从而在短时间内从循环中消失。
质粒DNA脂质体质粒DNA要在细胞内被有效地翻译,质粒DNA必须经过有效的细胞内运输进入细胞质,并从细胞质进入细胞核。编码白细胞介素12(一种具有抗**活性的细胞因子)的质粒DNA与阳离子脂质体配合,并在转移性肺*小鼠模型中测试其体内***作用。所研究的阳离子脂质体由全反式维甲酸(增强抗肿瘤作用)、DOTAP和胆固醇(摩尔比10:0.5:0.5)组成,与编码白介素12的质粒DNA配合。2次静脉注射质粒DNA(1.2mg/kg/只)后,与对照组相比,**结节和肿瘤细胞数量减少。在另一项研究中,应用由O,O-ditetradecanoyl-N-(α-trimethyl-ammonioacetyl)diethanolaminechloride(DC-6-14)、DOPE和胆固醇组成的阳离子脂质体递送表达miRNA7的质粒DNA。在携带酪氨酸激酶抑制剂耐药的异种移植**的小鼠身上测试了脂质体的***效果。**内注射阳离子脂质体复合物包封质粒(每只小鼠3ug)与注射乱码miRNA质粒DNA脂质体的小鼠相比,***抑制**生长。PAMAM树状大分子偶联,与DOPE(1:1)混合形成脂质体具有细胞核靶向功能。

非病毒载体通常具有比病毒载体更低的转染效率,但由于它们被认为要安全得多,因此已被***研究。纳米颗粒递送系统,其中阳离子脂质纳米颗粒通过核酸的负磷酸基团装载,是一类主要的非病毒载体,显示出高生产力和装载效率。用于携带核酸的纳米颗粒系统在整体上可分为基于脂质或聚合物的纳米颗粒,在与核酸相互作用后,每种纳米颗粒都被称为“脂质复合物”或“多聚体”。这些复合物的细胞递送被认为是通过内吞作用发生的,然后内体逃逸到细胞质中。阳离子脂质体作为核酸的一种传递系统,具有一定的优势。首先,阳离子脂质体在体内给药后是可生物降解的。内源性酶的存在可以分解脂质体的脂质成分。脂质体在各种纳米载体之间****的生物相容性导致在体内研究中使用阳离子脂质体递送各种sirna。脂质组成依赖性的表面电荷密度调节可以控制与带负电的核酸的相互作用力。聚乙二醇化脂质或功能性脂质的包含可以使脂质体的多种表面修饰成为可能。此外,在阳离子脂质体的脂质双层中包含亲脂性化学药物可以提供***药物和***性核酸的共递送。鉴于阳离子脂质体的优势,人们已经研究了阳离子脂质体用于递送各种核酸,如质粒DNA、反义寡核苷酸和siRNA。脂质体制备方法:薄膜⽔化法。山西脂质体载药给药
递送核酸的脂质体中的脂质成分有阳离子脂质、助脂、胆固醇结合DSPE-PGE2000等。陕西脂质体载药mRNA
microRNA脂质体
microRNA是真核细胞中发现的短(约22mer)非编码RNA,通过结合互补的mRNA序列发挥生物调节剂的作用。miRNA以初级miRNA的形式从其编码的核基因转录,其长度为数百个核苷酸。RNaseIII酶,Drosha,将初级miRNA加工成pre-miRNA(长度为70个核苷酸),携带一个特征的发夹环。然后pre-miRNA移动到细胞质中,在那里RNaseIII酶Dicer产生成熟的miRNA和乘客链。***,成熟的miRNA被整合到RNAi诱导的沉默复合体中,以降解它们的靶mRNA。由DOTMA、胆固醇和vitaminETPGS1k琥珀酸盐组成的阳离子脂质体被证明可以有效递送pre-miRNA-133b,导致A549非小肺*细胞中成熟miRNA-133b的表达比对照组细胞增加2.3倍,Mcl-1蛋白的表达减少1.8倍。经尾静脉注射含有pre-miRNA-133b的阳离子脂质体(1.5mg/kg)的ICR小鼠肺组织中成熟miRNA-133b的表达比接受含有紊乱的pre-mirna的阳离子脂质体的小鼠高52倍。 陕西脂质体载药mRNA
上一篇: 江西荧光染料蓝色
下一篇: 辽宁siRNA转染试剂